Introducción: el papel de las infecciones asociadas a la atención médica
La pandemia de gripe (H1N1) en 2009, la amenaza del virus del Ébola en África Occidental en 2014 y la Covid-19 en 2020 muestran que las amenazas internacionales a través de nuevas infecciones pueden surgir en cualquier momento. En particular, la pandemia de Covid-19 trajo un desafío sin precedentes a la salud pública, destacó la necesidad de invertir en sistemas de salud, estar preparados para gestionar las emergencias sanitarias mundiales y, posiblemente, para prevenirlas.
Las enfermedades infecciosas no sólo representan la principal causa de la crisis mundial, sino que siguen siendo la principal causa de muerte en todo el mundo, especialmente en los países de bajos ingresos y en los niños pequeños.
En 2019, dos enfermedades infecciosas -infecciones del tracto respiratorio inferior y enfermedades diarreicas- fueron clasificadas entre las diez principales causas de muerte en todo el mundo por la Organización Mundial de la Salud (OMS)1.
Paralelamente a las infecciones adquiridas en la comunidad, en los últimos años están surgiendo infecciones asociadas a la atención médica. Las Hai son aquellas infecciones que los pacientes adquieren mientras reciben atención médica»2.
Durante muchos años, la propagación de las infecciones ha sido vigilada de cerca por organismos nacionales e internacionales específicos, como el Centro para la Prevención y el Control de las Enfermedades (CDC) en América y en Europa (ECDC), con la misión de identificar, evaluar y comunicar las amenazas actuales y emergentes para la salud humana que plantean las enfermedades infecciosas.
Gracias a estos sistemas de vigilancia, las Ias más frecuentes notificadas en Europa son bien conocidas y se indican a continuación3:
Infecciones del tracto respiratorio (21.4% neumonía y 4.3% otras infecciones del tracto respiratorio inferior).
- Infecciones del tracto urinario (18,9%).
- Infecciones en el sitio quirúrgico (18.4%).
- Infecciones del torrente sanguíneo (10,8%).
- Infecciones gastrointestinales (8,9%),
con infección por Clostridium difficile que representa el 44.6% de este último (4.9% de todas las Ias).
En las últimas décadas, muchos hospitales han implementado programas de vigilancia y seguimiento, junto con estrategias de prevención sólidas, para reducir la tasa de Ias. Las infecciones nosocomiales a menudo están vinculadas a infecciones resistentes a los antibióticos y, por esa razón, tienen un impacto no solo en los individuos, en un solo paciente, sino también en las comunidades locales a las que pertenece este individuo.
La resistencia a los antimicrobianos (RAM) se refiere a la capacidad de los microorganismos para resistir los tratamientos antimicrobianos 4). El uso excesivo, el uso indebido y la autoadministración de antibióticos (especialmente en Italia, que ocupa el primer lugar en Europa junto con Grecia en muertes por resistencia a los antibióticos 5) se ha relacionado con la propagación de microorganismos resistentes a ellos, lo que hace que el tratamiento sea ineficaz y representa un grave riesgo para la salud pública.
A pesar de las muchas alarmas planteadas por la OMS y las múltiples campañas internacionales establecidas en todo el mundo, el número de muertes por resistencia a los antibióticos aumentó y crecerá cada año hasta alcanzar los 10 millones/ muerte por año en 20506.
El problema es que las bacterias no solo se vuelven resistentes a los antibióticos, sino que también pueden transferir la resistencia a futuras poblaciones bacterianas. Esto significa que la población de bacterias resistentes está creciendo tan rápido que los patógenos resistentes se extenderán rápidamente a entornos vinculados al ser humano (como aeropuertos, transporte público, escuelas, lugares de trabajo, gimnasios, etc.).
Para las infecciones causadas por bacterias, parece claro que la solución no se puede buscar aumentando el uso de nuevos antibióticos, sino desarrollando un plan integral y pautas para la prevención de las Ias, sistemas de diagnóstico más eficaces y oportunos, tanto en los centros de salud como en el hogar.
¿El cuidado en el hogar es un posible recurso?
Trasladar a los pacientes de la atención hospitalaria a la atención domiciliaria tendría una serie de efectos positivos, como una menor propagación de enfermedades infecciosas en el entorno, una reducción del riesgo de contraer infecciones por pacientes ya debilitados por enfermedades crónicas, una mayor disponibilidad de instalaciones clínicas para pacientes que necesitan especialmente ser hospitalizados y, finalmente, una reducción de los costos para los sistemas de atención médica7.
Ya a principios de 2000, se publicaron varias iniciativas de monitoreo remoto de pacientes para apoyar la capacidad de tratar a los pacientes en el hogar con el objetivo de mejorar la efectividad del tratamiento y el resultado asociado 8. En los años siguientes, la integración de la información clínica no homogénea en los flujos de trabajo de atención sanitaria ha comenzado a través de la adopción creciente de datos y estándares de interoperabilidad de procesos 9, lo que conduce al escenario actual donde, como se describe en el siguiente capítulo, las tecnologías modernas de salud digital podrían aportar un impulso sensible a la atención domiciliaria.
Esta sección describe tres escenarios de atención domiciliaria donde las tecnologías digitales ya están disponibles hoy en día integradas en el manejo de pacientes crónicos. Los programas de atención domiciliaria junto con herramientas digitales pueden ayudar a los profesionales de la salud a superar los aspectos críticos que podrían surgir al trasladar pacientes crónicos del hospital al territorio, y que podrían limitar (o incluso excluir) la aplicación de atención domiciliaria.
Nuestra experiencia se centra principalmente en la nutrición parenteral domiciliaria (HPN), la diálisis peritoneal (PD) y la terapia antibiótica parenteral ambulatoria (OPAT), pero hay muchas otras áreas terapéuticas donde la atención domiciliaria es aplicable hoy y aún más pronto.
Nutrición Parenteral en el Domicilio
La nutrición parenteral (PN) es una terapia para salvar vidas que se proporciona a través de la administración intravenosa (IV) de nutrientes (como aminoácidos, glucosa, lípidos, electrolitos, vitaminas y oligoelementos), fuera del tracto gastrointestinal. La nutrición parenteral total (TPN) es cuando la nutrición administrada por vía intravenosa es la única fuente de nutrición que el paciente está recibiendo.
Los principales efectos adversos asociados con la PN pueden deberse a anormalidades metabólicas, riesgo de infección o acceso venoso asociado10.
La transición de la nutrición parenteral hospitalaria a la basada en el territorio puede limitar/prevenir la exposición del paciente a infecciones nosocomiales, pero también puede plantear riesgos significativos y vulnerabilidades adicionales del paciente si estos no se monitorean y abordan sistemáticamente.
Como resultado, los beneficios del tratamiento de HPN pueden verse obstaculizados por complicaciones y eventos adversos que de otro modo serían evitables11.
Las formas en que las organizaciones de atención médica implementan la continuidad de la atención tienen un fuerte impacto en la seguridad de los programas de HPN.
Los riesgos para la seguridad del paciente en el momento del alta pueden ser altos y podrían conducir a una alta tasa de retorno al hospital12. Sin embargo, estos problemas pueden prevenirse adoptando estrategias adecuadas y protocolos claros 13. A menudo, los problemas críticos que determinan el reingreso del paciente que aumentan el riesgo para su seguridad son consecuencias directas de una falta de coordinación entre los sistemas territoriales y hospitalarios. Estas criticidades causan interrupciones en el flujo, gestión y coordinación de la información 14.
Las tecnologías digitales modernas (Figura 1) permiten la implementación de procesos automatizados a través de la introducción de plataformas web para la coordinación de actividades proporcionadas en el hogar del paciente (por ejemplo, asistencia de enfermería, materias primas, intercambio de datos clínicos) y la gestión de situaciones inesperadas con la posible participación de médicos hospitalarios y/o personal externo.
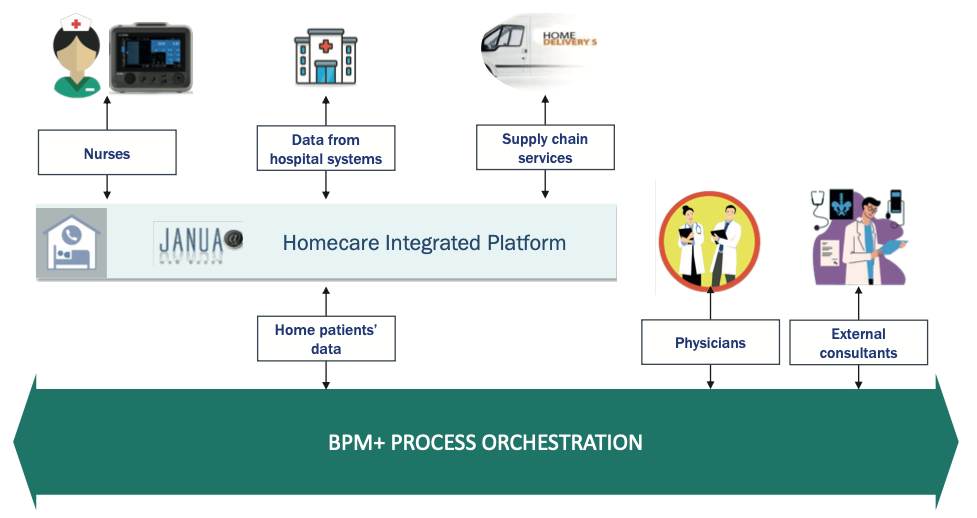
Fig. 1. Tecnologías digitales que apoyan el programa Parenteral Nutrition Home Care.
Un servicio HPN eficiente y eficaz solo puede proporcionarse mediante la implementación de una coordinación constante y oportuna de todas las actividades que van desde hacerse cargo del paciente hasta la adquisición de materias primas y la gestión administrativa relacionada de todo el proceso.
La adopción de una plataforma web diseñada para apoyar este proceso permite:
- Gestionar el continuo de atención en tiempo real.
- Compartir información en la transición del hospital al hogar y viceversa.
- Proporcionar una gestión integrada e ideal del paciente.
- Supervisar el desempeño del servicio prestado.
diálisis peritoneal
Además de los beneficios ya abordados derivados del entorno de atención domiciliaria, la posibilidad de manejar a los pacientes con enfermedad renal crónica sometidos a terapias de reemplazo renal en el hogar con diálisis peritoneal (PD) es un recurso precioso que permite a los pacientes llevar una vida casi normal.
La rápida evolución de la tecnología digital ahora abre las puertas a numerosas oportunidades, como la monitorización remota del paciente (RPM) mientras realiza la PD en casa con las últimas generaciones de ciclistas de PD (diálisis peritoneal automatizada, APD)15.
Durante la APD, los RPM con sensores inalámbricos permiten una adquisición constante de datos biométricos del paciente desde el ciclador durante toda la duración del tratamiento (Figura 2). El personal de atención médica (médicos dedicados y enfermeras de PD) puede ser asignado y autorizado para acceder a estos datos a través de PC/tabletas/teléfonos para monitorear los tratamientos de los pacientes en cualquier momento, desde cualquier lugar.

Fig. 2. Arquitectura del sistema APD.
Los ciclistas de nueva generación asignados hoy al paciente en casa, pueden comunicarse de forma autónoma con el Hospital (donde se encuentra el centro clínico operativo) y permitir la recopilación de datos del paciente al final de cada tratamiento APD.
Los datos recopilados del paciente, tanto biométricos como relacionados con el tratamiento de APD, son constantemente analizados por el Sistema y pueden transformarse en alarmas/alertas para los profesionales de la salud responsables del manejo del paciente.
Los médicos y enfermeras pueden verificar de forma remota los datos de los pacientes y decidir cambiar el régimen/ prescripción de PD de forma remota, si es necesario.
El impacto de adaptar los tratamientos/recetas médicas de forma remota puede aumentar el cumplimiento del paciente, optimizar los resultados de los pacientes y mejorar la seguridad de los pacientes.
Además de eso, evitar múltiples accesos de los pacientes a su hospital de referencia para revisar/cambiar los tratamientos, tiene el potencial de reducir la carga sentida por las familias que brindan atención en el hogar, mejorar la adherencia al tratamiento y a través de bucles de retroalimentación en tiempo real para mejorar el conocimiento a través de la educación individualizada.
Terapia con antibióticos parenterales para pacientes ambulatorios
El concepto de terapia antibiótica parenteral ambulatoria (OPAT) nació a principios de la década de 1980 en los Estados Unidos con el objetivo de reunir una reducción de costos y una mejora en la calidad de vida del paciente como resultado de una estancia hospitalaria más corta, y de un entorno más acogedor y cómodo que rodea al paciente|||UNTRANSLATED_CONTENT_START|||16.|||UNTRANSLATED_CONTENT_END|||
Sin embargo, para que el OPAT sea realizado de forma independiente por el paciente, se deben garantizar los siguientes pasos:
- Corrección de la dosificación del fármaco y sus componentes.
- Ausencia de contaminación ambiental.
- Tasa correcta de administración.
Hoy en día es posible gestionar el OPAT a través de un proceso basado en el hogar (Figura 3) y la adopción de tecnologías biomédicas modernas.
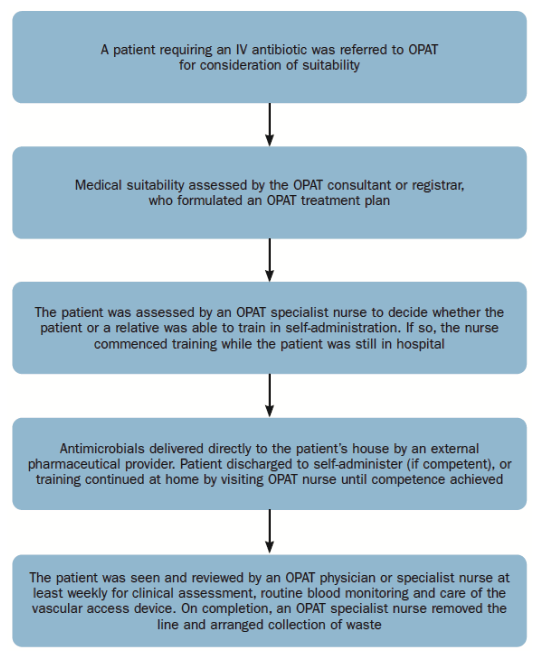
Fig. 3. Proceso basado en el hogar OPAT
Con el uso de estas tecnologías innovadoras, los pacientes/ cuidadores que no son capaces de mezclar los antimicrobianos de la manera tradicional, pueden ser entrenados en el uso de dispositivos elastoméricos rellenos asépticamente premezclados por proveedores farmacéuticos externos.
Usando dispositivos de infusión continua de 24 horas, los antibióticos betalactámicos como flucloxacilina, bencilpenicilina y piperacilina con tazobactam pueden ser autoadministrados por los propios pacientes, evitando el hospital durante la duración de la terapia.
Los pacientes ancianos o con problemas de destreza, los pacientes con regímenes complejos y multifármacos y aquellos para quienes los antibióticos betalactámicos continuos fueron el tratamiento preferido ahora pueden ser des-hospitalizados al proporcionarles un dispositivo elastomérico, que contiene un «balón» elastomérico: a medida que se desinfla con el tiempo, empuja suavemente el antimicrobiano a través del equipo de infusión intravenosa que lleva el fármaco desde el dispositivo al catéter/puerto, proporcionando una velocidad de flujo confiable y precisa.
Tecnologías de salud digital presentes y futuras para el manejo de infecciones
Las tecnologías digitales modernas son recursos valiosos para hacer frente a la propagación de infecciones y apoyar la transición del hospital al hogar del paciente.
La implementación de dispositivos digitales tanto en el entorno hospitalario como en el hogar, puede:
- Facilitar la identificación temprana del riesgo de infección y permitir la pronta intervención del personal médico y de enfermería.
- Permitir un manejo más prudente de los antibióticos de amplio espectro, prevenir más eficazmente la resistencia a los antibióticos y mejorar el tipo y las dosis de la terapia antimicrobiana adecuada.
- Maximizar la bioseguridad ambiental.
- Garantizar la gobernanza de los servicios terapéuticos prestados al territorio, gracias al monitoreo del desempeño en tiempo real.
En los párrafos siguientes se describen algunos ejemplos de estas tecnologías.
Plataforma web para la vigilancia de infecciones
Hasta hace pocos años, las actividades de vigilancia de infecciones eran realizadas por equipos médicos interdisciplinarios que analizaban datos extraídos de diversos sistemas de información hospitalaria como, por ejemplo, la Historia Clínica Electrónica y/o el Sistema de Información de Laboratorio (LIS).
Hoy en día, la emergencia sanitaria relacionada con las infecciones hospitalarias causadas por la resistencia a los antibióticos pone el foco en los equipos de vigilancia sanitaria, que han aumentado la necesidad de una extracción automatizada y más frecuente de un número creciente de datos clínicos no homogéneos.
Los proveedores de sistemas de información médica están rezagados en la innovación en la vigilancia de infecciones, lo que ha llevado a muchas organizaciones de atención médica a equiparse con herramientas específicas para la vigilancia y el control avanzado de infecciones 17.
Una plataforma específica de vigilancia de infecciones debe ser capaz de recopilar datos de manera transparente de cualquier sistema de información existente dentro de una organización de atención médica: registro de admisión, alta y transferencia de pacientes, laboratorio de microbiología, quirófanos, equipos médicos, radiología, etc.
Los datos recopilados son procesados por algoritmos capaces de detectar inmediatamente riesgos potenciales tales como:
- La presencia, en un tiempo determinado, de dos o más casos de un microorganismo infeccioso detectado en pacientes hospitalizados en la misma sala.
- El reingreso de un paciente que tuvo una infección grave en el último año.
Cuando se produce un riesgo potencial de infecciones, se notifica con prontitud al personal de vigilancia para que se puedan tomar las precauciones adecuadas para evitar la aparición de grupos epidémicos.
Además, estos sistemas también pueden proporcionar un apoyo válido en la administración de antimicrobianos. Como ejemplo, la prescripción de un antibiótico de amplio espectro podría interrumpirse de inmediato a favor de un fármaco dirigido tan pronto como el laboratorio genere un informe válido que confirme que se ha identificado un microorganismo patógeno específico.
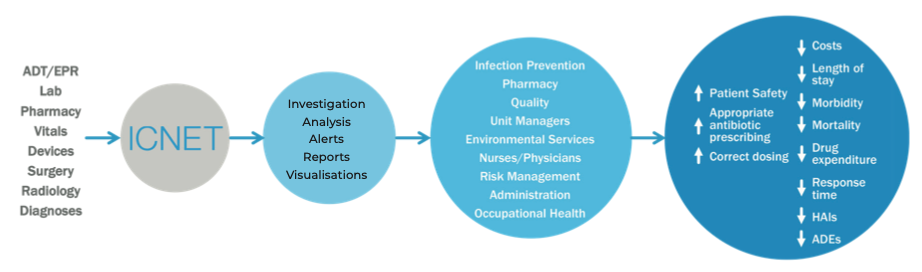
Fig. 4. Esquema de funcionamiento de la plataforma de vigilancia de infecciones ICNet
Dicha plataforma puede traer grandes beneficios dentro de un centro de salud, como reducir las infecciones del sitio quirúrgico (SSI)18, reducir la carga de trabajo del equipo de vigilancia de infecciones 19 y disminuir significativamente la prescripción de antibióticos de amplio espectro 20 y el uso de antibióticos en general21.
La adopción de una plataforma específica para la vigilancia de las infecciones permite un mayor control en el manejo de los pacientes y, en consecuencia, favorece el posible desplazamiento del hospital al territorio, por ejemplo para el tratamiento de pacientes crónicos y/o para la fase postoperatoria.
Dispositivos para desinfectar habitaciones utilizando tecnología de iluminación
Si bien proporcionar terapias en el hogar del paciente proporciona todas las ventajas descritas en los párrafos anteriores, el entorno del hogar puede no ser capaz de garantizar condiciones de bioseguridad adecuadas. Por esta razón, en el caso de pacientes particularmente delicados o críticos, podría ser útil adoptar un sistema que permita la sanitización continua de los entornos.
Se han desarrollado algunas tecnologías muy prometedoras basadas en el concepto de sanitización continua utilizando frecuencias de luz visible, sin emisión de radiación ionizante cero, que, mientras iluminan las habitaciones, las sanitizan continuamente. Estas tecnologías están diseñadas para proporcionar desinfección sin esterilizar el medio ambiente y controlar la proliferación de bacterias y virus que actúan en sinergia con la resiliencia natural del sistema inmunológico humano.
Esta tecnología se basa en las siguientes premisas22:
- Evite la «recontaminación». La “recontaminación” es el restablecimiento de una población microbiana potencialmente patógena en ambientes que previamente han sido tratados con desinfectantes químicos; como se puede imaginar fácilmente, una vez que una superficie o un ambiente ha sido tratado a través de sistemas de sanitización física o química, es inevitable que sea recontaminado tan pronto como los seres vivos comiencen a visitarlo.
- Contrarrestar el fenómeno del “resistome” (el resistome es el material genético intercambiado entre microorganismos que permite la adquisición de información genética favoreciendo la resistencia a los antibióticos). El uso imprudente de desinfectantes y antibióticos favorece la fijación en diferentes poblaciones de microorganismos y mutaciones que los protegen a expensas de los sensibles. De esta manera ocupan espacios de vida cada vez más grandes y se vuelven fijos.
- Concepto de antagonismo competitivo. No elimina todos los microorganismos de forma incontrolada, pero, si bien elimina los gérmenes patógenos, favorece el establecimiento de colonias estables de “probióticos”.
- La tecnología es «personalizable», se puede calibrar para garantizar la efectividad requerida por entornos con diferentes niveles de riesgo microbiológico.
Se descubrió que esta tecnología era efectiva en diferentes tipos de bacterias GRAM+ y gram-, virus (incluido el SARS-Cov-2), hongos, esporas y mohos, tanto en pruebas in vitro como in vivo 23.
Simplemente reemplazar las luces con este tipo de dispositivo le permitirá aumentar el nivel de bioseguridad de los ambientes, reduciendo cualquier riesgo residual de contaminación y maximizando su efectividad.
Además, estas tecnologías se pueden integrar con sensores IoT alimentados a través de la red Ethernet (PoE = Power over Ethernet) que ofrecen las siguientes ventajas:
- Conexión de bajo voltaje, fácil instalación.
- Integra la tecnología de luz desinfectante descrita anteriormente.
- Detección de presencia, temperatura, humedad, COV (Compuesto Orgánico Volátil), luz ambiente, CO2.
- Integre luces indicadoras para admitir muchos casos de uso.
- Permiten identificar y mostrar el nivel de ocupación de una habitación, definir ciclos de saneamiento, gestionar trayectorias clínicas y alertas.
Orquestación del proceso de atención médica
Siempre que se traslade una vía clínica del hospital al territorio, es necesario adoptar herramientas que garanticen su gobernanza, es decir, herramientas que permitan la ejecución efectiva y oportuna, y la sincronización de las actividades entre todos los operadores involucrados, aumentando la eficiencia relacionada.
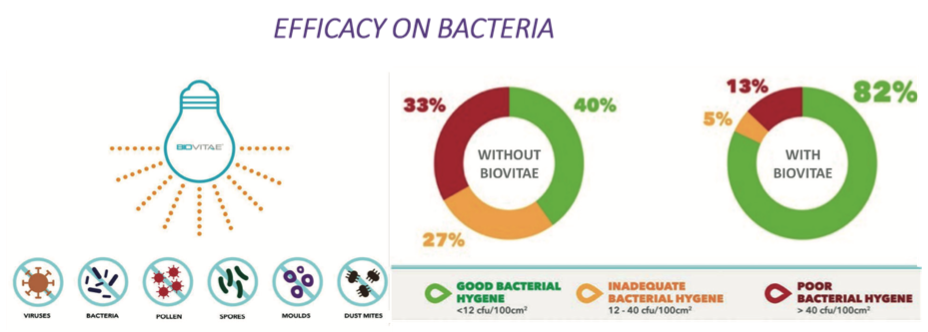
Fig. 5. Resultados de la aplicación de las luces Biovitae en bacterias.
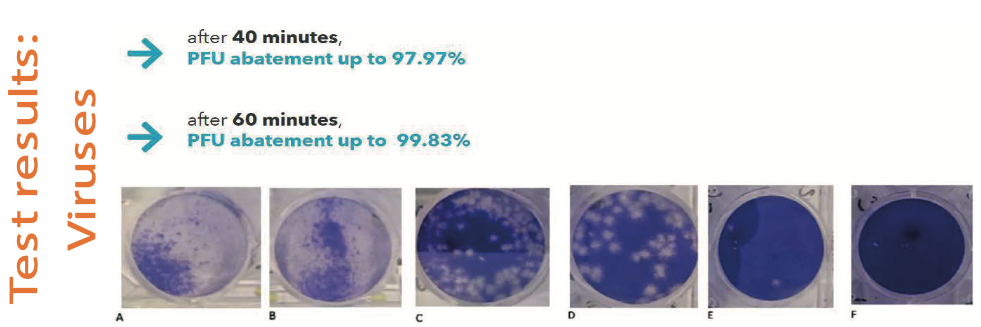
Fig. 6. Resultados de la aplicación de luces Bioviae en virus.
Este nivel de sincronización -o “orquestación” – es posible gracias al uso de capas tecnológicas ya disponibles hoy en día:
- Un repositorio común donde agregar todos los datos clínicos recopilados.
- Un esquema semántico común que garantiza el mantenimiento de los datos durante las interacciones entre todos los operadores y sistemas involucrados.
- Un medio por el cual los diversos sistemas de información pueden compartir no solo datos e información, sino también elementos contextuales como eventos y metadatos (es decir, datos relacionados con datos que proporcionan una descripción del contexto).
- La descripción de las interacciones entre todos los operadores involucrados a través de una notación estándar que permite una descripción correcta y precisa del proceso y su implementación y sincronización.
A través de este enfoque24, será posible implementar una herramienta centralizada e integrada a través de la cual se cuide a los pacientes a domicilio: una vez que un paciente haya sido enmarcado en una de las posibles vías de atención domiciliaria, será suficiente crear una nueva instancia de la vía orquestada adecuada y todos los sistemas y operadores involucrados serán informados de manera rápida y oportuna sobre lo que se espera de ellos.
Además, será posible analizar el rendimiento del proceso en tiempo real: será posible detectar cuellos de botella, medir el tiempo de ejecución de cada ruta y medir constantemente indicadores clave de rendimiento (KPI) específicos para asegurarse de que el servicio proporcionado se alinea con los requisitos.
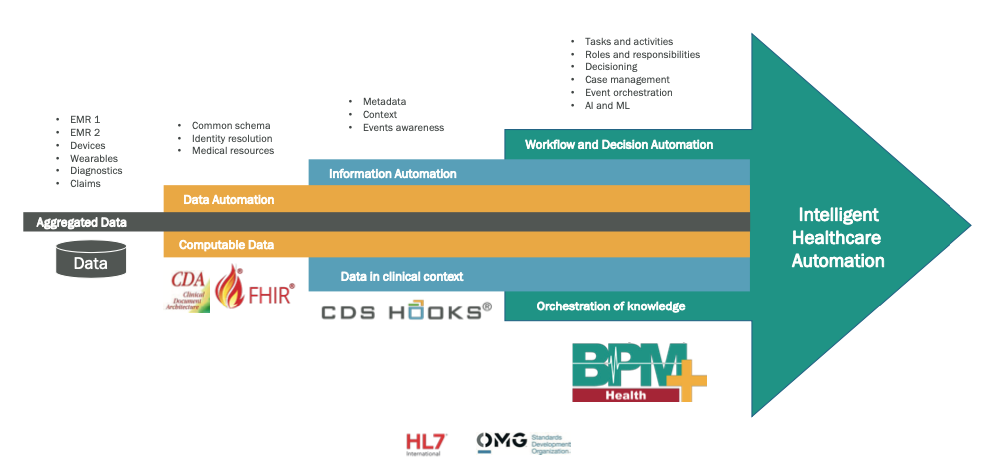
Fig. 7. Capas digitales que componen un sistema inteligente de automatización sanitaria.
Conclusiones
Las enfermedades infecciosas pueden ser controladas, y con suerte prevenidas, a través de la implementación de programas globales de vigilancia y educación en los centros de salud y la creación de conciencia en la población en general.
además de eso, la clara inversión global, el desarrollo y la adopción de tecnologías digitales pueden apoyar al sistema de salud mundial y a los proveedores de atención médica para reducir/gestionar las Ias y, al mismo tiempo, aumentar/garantizar gramos a los usuarios bien educados/ya disponibles hoy en día: prevenir/controlar el acceso a las infecciones de los pacientes programados para la atención domiciliaria.
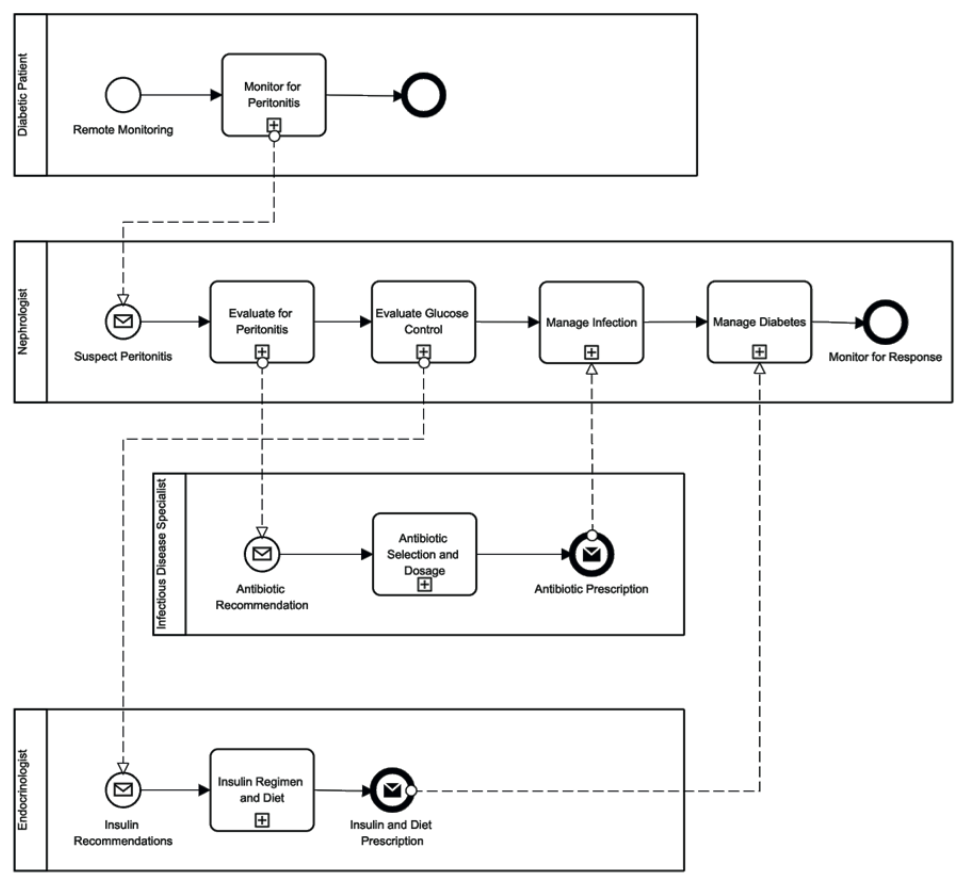
Fig. 8. El modelo BPMN de la vía de atención médica se centró en los pacientes diabéticos inscritos en un programa de APD.